研究案内
腫瘍
基礎研究
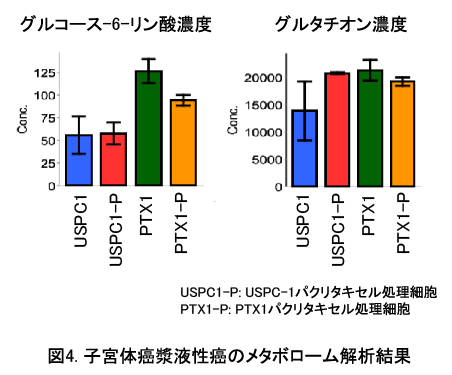
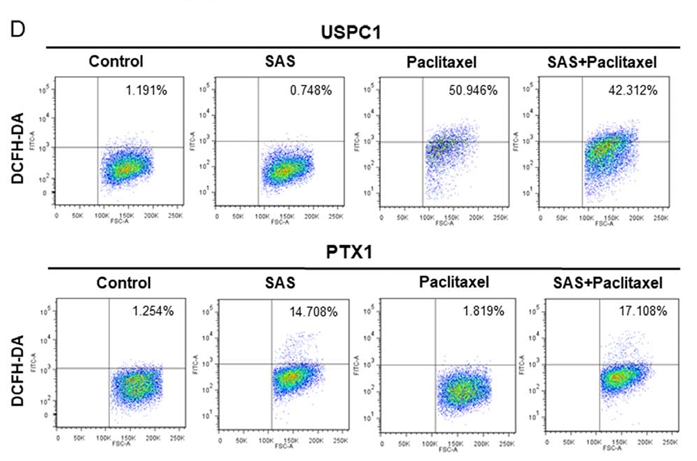
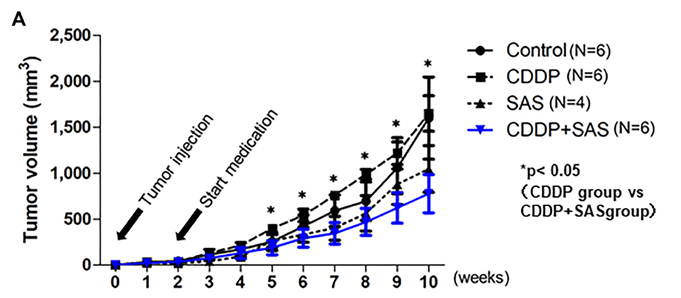
当研究室では以前より、子宮体癌の中でも治療困難であることが多い子宮体部漿液性癌について研究を進めています。私達は抗癌剤に対する子宮体部漿液性癌細胞の反応をメタボローム解析という手法を用いて解析を行いました。メタボローム解析は近年癌の研究分野で広く行われ始めた研究手法です。細胞は様々なシグナル伝達を受け多くの代謝反応を行いますが、メタボローム解析ではその代謝過程~最終産物を解析します。癌細胞の代謝産物を解析することで、癌細胞の代謝経路の性質・特徴を解し、治療法の開発に役立てることができます。子宮体部漿液性癌は一般的には抗癌剤耐性であることが多いのですが、当科ではパクリタキセルの耐性株(東北大との共同研究)を用いて、パクリタキセル耐性細胞の代謝経路変化を調べました。その中で注目されたのが、グルタチオン経路と糖代謝経路です。これまで他癌腫ではグルタチオン・糖代謝のいずれの代謝経路も抗癌剤耐性に関わっているということが分かっていましたが、これらが子宮体部漿液性癌のパクリタキセル耐性にも関与する可能性を世界で初めて報告しました(Seino M, Oncotarget 2018)(図1)。メタボローム解析結果を基に、子宮体部漿液性癌の新規治療ターゲットについてさらに研究を進め、潰瘍性大腸炎の治療薬であるスルファサラジンを用いてグルタチオン代謝経路を抑えることでパクリタキセル耐性細胞を効果的に抑制するという成果を報告しています(Akiko S, Oncol Lett. 2020)(図2)。この研究成果は2017年に行われた日本産科婦人科学会で、優秀演題賞を獲得しました(杉山)。ここからさらに研究を進め、グパクリタキセルのみならず、子宮体漿液性癌細胞株においてスルファサラジンがシスプラチンの抗腫瘍効果を増強することを報告しています(Kanako S, Oncotarget. 2022)(図3)。さらに、子宮体部漿液性癌のみならず、卵巣癌において代表的な治療抵抗性である明細胞癌細胞株においても同様の検討を行い、グルタチオン代謝経路と細胞死誘導に関する検討を行い、スルファサラジンとパクリタキセルの併用により抗腫瘍効果が増強することを報告しております(Urara Idei, Int J Mol Sci. 2023)(図4)。
このように一つの研究から、発展を重ね多くの若手医師が研究を続け次々と画期的な報告を行っています。
現在の最新の研究としては、このメタボローム研究を臨床研究へと発展させています。
その他の基礎研究として、卵巣癌におけるPARP(Poly ADP-Ribose polymerase)阻害薬を増強するための探索的研究を行っています。PARP阻害薬は、近年卵巣癌治療に導入された新規分子標的薬であり、卵巣癌の治療成績を大幅に改善させることが期待される薬剤です。しかし一方で、このPARP阻害薬に対する高い感受性が遺伝子発現から予想される患者様でも、治療抵抗性を示す方がいます、本研究室では、山形大学創薬研究拠点(YU-COE(S))で開発された化合物ライブラリーを用いて、多数の化合物とPARP阻害薬を併用することでPARP阻害薬の治療効果を増強することのできる薬剤を検索しています。この研究の長所は、用いている薬剤はすでに臨床応用がされている薬剤であり、基礎研究で効果が認められた場合、早期の臨床試験及び臨床応用が期待できる点です。
また、同様にPARP阻害薬に注目した実験として、Schlafen11遺伝子とPARP阻害薬に関する検討を行っています。再発卵巣癌においてSchlafen11遺伝子とPARP阻害薬の治療効果に相関関係があることを第65回婦人科腫瘍学会にて報告しております。今後は初発卵巣癌についても研究を進めていく予定です、
臨床研究
私達の研究室では、臨床研究も行っております。単一施設の限られた症例数では臨床研究で成果をあげることは難しいのですが、患者さん一人ひとりのデータを丁寧に分析することで、臨床データを論文化することができると考えています。
我々は閉経後の一般的な卵巣腫瘍患者において、実に44%(75例中33例)もの高率に血清エストラジオール(E2)濃度が高いことを見出しました。卵巣静脈採血を行って卵巣静脈血のE2濃度を測定したところ、健側の卵巣静脈に比較して患側の卵巣静脈中のE2濃度が有意に高く、また免疫染色により卵巣腫瘍間質に性ホルモン合成酵素の発現を認めたことから、極めて高頻度に卵巣腫瘍の間質でE2が産生されていること、さらに産生されたE2が骨代謝に影響を与えていることを明らかにしました(Matsumura S, J Clin Endocrinol Metab 2013)。この研究は、日々の臨床の中で疑問に思ったことから始まり、若手医師がまとめた研究です。
現在は新たなテーマとして、基礎研究から発展させたメタボローム解析を用いた唾液を用いた新規卵巣癌マーカーの発見に関する研究を行っています。これは従来の採血より、より簡便でかつ非侵襲的な検体採取が可能な唾液に着目し、卵巣癌の早期発見や治療標的となる新規分子の発見を試みる画期的な研究です。
また手術中にインドシアニングリーン(ICG)を含む色素を用いたセンチネルリンパ節の同定について研究を進めております。センチネルリンパ節とは、癌細胞が最初に到達するリンパ節のことを言います。子宮に色素を注入し、リンパ流を手術中に観察することでセンチネルリンパ節を同定し摘出します。摘出したセンチネルリンパ節は細かくスライスし、小さな癌も見逃さないようにします。本来リンパ節転移の有無を確認するためにリンパ節郭清(可能な限りすべてのリンパ節を摘出すること)が必要ですが、癌細胞が最初に到達するセンチネルリンパ節が同定でき、そのセンチネルリンパ節に癌の転移がないことが証明できれば、それ以降のリンパ節には転移がないと判断でき、リンパ節郭清を省略できる可能性があります。リンパ節郭清には、リンパ浮腫やリンパ嚢胞といった術後合併症が起こりえますので、それらの合併症を軽減できるのではないかと考えられています。私たちはセンチネルリンパ節を安定して同定できるように研究を進めています。
さらに私達は、婦人科悪性腫瘍研究機構(JGOG)や東北婦人科腫瘍研究会(TGCU)が主体となって行われる多施設共同研究にも積極的に参加しています。JGOGでは難治性卵巣癌の治療研究や卵巣癌の相同組み換え修復異常の頻度とその臨床的意義を明らかにする臨床研究など、多数の調査に協力しています。JGOG1082試験では子宮頸癌術後の再発高リスク群に対して同時化学放射線治療と化学療法の再発抑制効果の比較検討を行っています。JGOG2051試験では子宮体癌において、妊孕性温存療法(MPA療法)後に再発した症例において再度のMPA療法の有効性について検討を行う試験です。PEACH Studyは子宮体癌術後化学療法施行例における再発後の化学療法について従来のプラチナ系製剤併用レジュメと近年新たに治療選択肢となったレンバチニブ・ペムブロリズマブ併用療法、そしてペムブロリズマブ単剤療法の治療予後を前向きに比較する試験です。JGOG3024試験は、家族性乳癌卵巣癌症候群(HBOC)の症例の経過を前向きに観察する試験です。JGOG3031試験は再発卵巣癌におけるニラパリブ維持療法の有効性を検討する前向き試験になります。
当院が中心となりTGCUでは子宮頸癌における同時化学重粒子線治療と従来の同時化学放射線治療との治療成績や副作用を比較するための調査研究を行っております。多施設での研究は単一施設では何年もかかるような疾患でも短期間で集めることができ、その豊富な症例数により婦人科腫瘍における疑問点を解決し、新しい標準治療法を確立できる可能性があります。そのため私達は、研究に参加するにあたり、質の高いデータを提供するように心がけています。また私達からも新規臨床試験のアイデアを発信できるようになりたいと、カンファレンスで日常診療の疑問点をdiscussionしております。
最後に私達の研究室では、永瀬教授を中心として卵巣癌、子宮体癌のほかに子宮頸癌の新規研究も立ち上げようとしています。特に若手医師が疑問に思ったことを積極的に臨床研究につなげていければと考えています。当科では医学部生の課外実習も受け入れており、臨床研究や基礎研究を共に行っています。厳しいなかにも笑いあり、アットホームな環境です。産婦人科でがんの研究をしたいと考えている学生さん、若手医師が、私達の仲間となってくれることを期待しています。